江 波, 孙文寿, 蔡 杰
(1. 青岛大学环境科学与工程学院, 山东 青岛 266071;
2. 潍坊西恩能源技术有限公司, 山东 潍坊 261000)
钢材具有价格便宜、力学性能好等优点,具有广泛的应用[1]。
但钢材存在易腐蚀的缺点[2]。
目前,在工业设备中较为常见的防腐蚀方法是向设备中投加缓蚀剂,该方法操作简便,保护效果好[3]。
有机胺类缓蚀剂价廉易得,防腐性能优良,广泛用于金属防腐。
但其溶解度低,使用过程中存在乳化效果差、分散不均匀等诸多问题[4]。
相关研究表明,可通过与其它药剂复配的方式,解决这些问题[5,6]。
选择的复配药剂要满足绿色环保的要求。
N-油基-1,3-丙撑二胺(NOPDA)是一种不饱和有机胺,分子中含有2 个氨基和1 个C =C 键,能够有效地吸附在金属表面,形成保护膜,从而起到抑制腐蚀的作用。
但其溶解度低,单独使用时效果不佳。
二乙氨基乙醇(DEAE)性质稳定,常被用作乳化剂等,研究表明[7],DEAE 是一种相对环境友好的复配成分。
为此,本工作以NOPDA 和DEAE 为主剂,制得安全环保的缓蚀剂,命名为FFA,采用静态失重法研究了FFA 在1 mol/L 盐酸溶液中对20 碳钢的缓蚀作用,探究了温度及投加量对缓蚀效果的影响,通过拟合等温吸附曲线分析了缓蚀剂的作用机制,通过EIS 测试、观察SEM 以及AFM 表面形貌分析了缓蚀剂在盐酸溶液中对20 钢的缓蚀效果。
采用50 mm×25 mm×2 mm 的20 碳钢试片作为腐蚀试片,其成分见表1。
以1 mol/L 盐酸溶液作为腐蚀溶液。
取盐酸溶液(浓盐酸和水的体积比为1 ∶4)1 000 mL,加入8 g 六次甲基四胺,制成酸洗溶液备用。称取60 g NaOH 固体,溶于适量蒸馏水中,转移至1 000 mL 容量瓶中定容,制成碱洗溶液备用。
除NOPDA 为工业级外,DEAE 等其他药品均为分析纯。

表1 20 碳钢试片化学成分Table 1 Chemical composition of the 20 carbon steel test piece
在80 ℃的条件下,依次将NOPDA、DEAE、表面活性剂、水添加到带有回流装置的三口烧瓶中,边加边搅拌,1 h 后取出制得溶液,待冷却至室温即可使用。
制得的FFA 中NOPDA 和DEAE 的含量分别为2.5%(质量分数,下同)和15.0%,表面活性剂的含量为21.0%,其余为水。
该缓蚀剂通过复配制得,故制备时各有机物的量与成品FFA 中的量一致,因此未赘述制备FFA时各药品的加入量。
用不同目数(400、600、800、1 000、1 200、1 500,2 000目)的金相砂纸打磨碳钢表面,再依次用蒸馏水洗涤,用丙酮擦拭以脱脂,用乙醇洗涤,置于纯净的无水乙醇中浸泡1 min 后,取出用冷风吹干,在干燥器中干燥4 h,保存备用。
用电子天平(精度为0.000 1 g)准确称重20 碳钢试样后,将其浸入含有不同浓度FFA 的1 mol/L 盐酸溶液中。
4 h 后取出试样,依次用蒸馏水、酸洗溶液、碱洗溶液和无水乙醇洗涤试样,然后在干燥器中干燥,4 h 后取出称重[8,9]。
为减小误差,所有实验平行进行3 次。
用式(1)计算腐蚀率v[10,11]:
式中:v为腐蚀速率,mm/a;
W1和W2分别是腐蚀实验前、后试样的质量,g;
s为碳钢试样表面积,cm2;
t为腐蚀时间,h;
ρ为碳钢试样的密度,g/cm3。
缓蚀率η计算如公式(2)[12]:
式中:η为缓蚀率;
v0和v1分别为在不含有和含有FFA情况下试样的腐蚀速率。
缓蚀剂在金属表面的吸附类型通常分为物理吸附和化学吸附。
通过拟合等温吸附数据,可以推断吸附机理。
缓蚀剂的作用是防止金属腐蚀,因此,可假设被缓蚀剂覆盖的地方不会被腐蚀,可以用缓蚀率代表碳钢表面覆盖度θ,即θ值的大小可以用η值来表示[13,14]。
在298~353 K 温度范围内,在FFA 投加量为0~10 g/L 的范围内测定了FFA 的缓蚀率,考察吸附等温线,腐蚀时间控制在4 h,根据实验结果,得出吸附平衡常数,并分析FFA 的吸附机制。
电化学阻抗谱(EIS)是评价缓蚀剂性能的有效方法之一。
EIS 测试在CHI750E 电化学工作站上进行。工作电极为20 碳钢试片(表面积为12.5 cm2),辅助电极为铂片,参比电极为Ag/AgCl 电极。
为获得稳定的开路电压,工作电极要在含有不同浓度FFA 的1 mol/L HCl 溶液中浸泡30 min,将工作电极、参比电极和辅助电极装入电解池中,使碳钢试样尽量平行于参比电极,减少测量误差。
预热电化学工作站20 min,扫描频率为1.0×(10-1~104) Hz,测试在室温条件下进行,采用Zsimp 软件对阻抗数据进行拟合分析。
将20 碳钢试样浸入不含或含5 g/L FFA 的1 mol/L盐酸溶液中,水浴温度为60 ℃,4 h 后取出。
然后用少量蒸馏水冲洗试样,冷风干燥后储存在干燥器中待测。
1.6.1 接触角测试
在室温下用JY-PHb 接触角测定仪测定试样的接触角。
将0.16 mL 去离子水滴在试样表面,5 s 后,测量静态接触角。
在试样表面的不同位置平行进行3 次测量,以减少误差。
1.6.2 SEM 分析
采用TM300 台式扫描电镜在放大倍数为2×103的条件下测试碳钢表面的形貌,以进一步观察缓蚀剂的缓蚀效果。
1.6.3 AFM 分析
采用Nanoscope V Multimode 8 原子力显微镜(AFM)测试试样的2D、3D AFM 形貌,扫描面积为100 μm2,温度为25 ℃,相对湿度为25%。
图1 中,v0曲线为未投加缓蚀剂的空白组的腐蚀速率随温度的变化曲线,v及η曲线分别为FFA 投加量为5 g/L 时试样的腐蚀速率和缓蚀率随温度的变化曲线。
观察图1 发现,随着温度的升高,缓蚀率先增加后趋于平缓,当温度达到343 K 时,缓蚀率最高为94.5%。这是因为随着温度的升高,缓蚀剂分子的运动速率加快,缓蚀剂分子吸附在碳钢试片表面的可能性就越大,对碳钢试片的保护效果就越好,即缓蚀率越高。
同时,腐蚀速率随温度的升高而加快,当温度小于343 K 时,腐蚀速率v0和v随温度缓慢增大,当温度由343 K 增加到353 K 时,腐蚀速率v0和v的增大明显加快,其中v由3.67 mm/a 增大到9.47 mm/a。
这也解释了为何在温度较高时,缓蚀率趋于平缓并有下降趋势。

图1 温度对腐蚀速率和缓蚀率的影响Fig. 1 Effect of temperature on corrosion rate and corrosion inhibition efficiency
图2 为温度为343 K 时腐蚀速率v和缓蚀率η随FFA 的投加量c的变化曲线。
由图2 可知,随着投加量的增加,缓蚀率先增加后趋于减少,当FFA 的投加量为5 g/L 时,缓蚀率最高为94.5%。
腐蚀速率随着投加量的增加逐渐减小后趋于增加,与缓蚀率的规律恰好相反。
这是因为随着投加量的增加,系统中起保护作用的分子增加,吸附在碳钢试片表面的缓蚀剂分子增多,缓蚀率增加。
当FFA 的投加量达到5 g/L 时,缓蚀剂在金属表面的吸附达到平衡,表现为此时η最大,v最小,因此,FFA 的最佳投加量为5 g/L[15]。
当投加量超过5 g/L 时,系统中FFA 分子过多,分子之间的相互斥力增大,出现浓度极值现象[16],保护效果降低。
当投加量为0.5 g/L 时,缓蚀率也达到了85.0%,此时缓蚀剂中NOPDA 含量为12.5 mg/L,DEAE 含量为75.0 mg/L。
缓蚀剂用量宜根据其实际应用情况来确定。
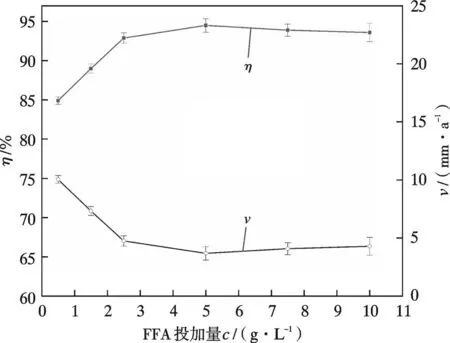
图2 FFA 投加量对腐蚀速率和缓蚀率的影响Fig. 2 Effect of FFA dosage on corrosion rate and corrosion inhibition efficiency
Langmuir,Frumkin 和Temkin 等不同的等温吸附模型均可用于拟合失重试验数据[17], 其中Langmuir 模型(式3)是最常用的模型:
式中:C为FFA 的物质的量浓度,mol/L;
θ为覆盖度;
Kads是吸附平衡常数。
1 mol/L HCl 中不同温度下η随c的变化见图3。以Langmuir 模型拟合不同温度下的等温吸附数据,结果如图4 所示。
由图4 可知,C/θ与C呈良好的线性关系。
表2 为1 mol/L HCl 中FFA 在碳钢上的吸附热力学参数。
由表2 可知,不同温度对应的R2均趋近于1,这表明缓蚀剂在碳钢表面的吸附符合Langmuir 等温吸附模型。
由式(3)可知,由拟合直线在C/θ轴上的截距可以得出吸附平衡常数Kads,再根据式(4)[18]可得吉布斯自由能ΔGads,结果列于表2。

表2 1 mol/L HCl 中FFA 在碳钢上的吸附热力学参数Table 2 Thermodynamic parameters for the adsorption of FFA inhibitor on carbon steel in 1 mol/L HCl

图3 1 mol/L HCl 中不同温度下η 随c 的变化Fig. 3 Variation of η with c at different temperatures in 1 mol/L HCl

图4 1 mol/L HCl 中FFA 在碳钢上吸附的Langmuir 等温线Fig. 4 Linearized Langmuir isotherms for the adsorption of FFA inhibitor on carbon steel in 1 mol/L HCl
式中:55.5 是水分子的浓度,mol/L;
R是理想气体常数;
T是绝对热力学温度,K。
通常认为,当|ΔGads|≤20 kJ/moL 时,缓蚀剂分子在金属表面上的吸附主要是静电力相互作用的物理吸附;
当|ΔGads|≥40 kJ/moL 时,主要是化学吸附,涉及到配位共价键的形成,当|ΔGads|在20~40 kJ/moL 之间,物理吸附和化学吸附同时存在[19]。
从表2 中可以看出,ΔGads的绝对值在20~40 kJ/mol 之间,并且随温度的升高而增加,因此,FFA 的吸附过程既有物理吸附也有化学吸附。
ΔGads<0 表明FFA 在20 碳钢表面的吸附是自发过程。
根据Van’t Hoff 公式[式(5),其中a为常数]作图(图5)可得到ΔHads的数值,根据式(6)计算ΔSads,结果见表2。

图5 lnKads随1 000/T 的变化曲线Fig. 5 lnKads versus 1 000/T curve
ΔHads>0,证实了FFA 分子在20 碳钢表面的吸附是吸热过程,这也解释了为什么2.1 节图1 中缓蚀剂的缓蚀率随着温度的升高先增加后趋于平缓。
ΔHads>0 表明提高温度对吸附有利。
ΔSads>0 且在不同温度下无明显变化,这意味着FFA 分子吸附到试片表面所导致的熵减小小于水分子等从金属表面脱附所导致的熵增量[20]。
图6 和图7 分别为不同FFA 投加量下试样在1 mol/L HCl 中的电化学阻抗谱和对应的等效电路,分析得到相应的电化学参数见表3。
等效电路图中的Rs为溶液的电阻,Rt为碳钢试样的电荷转移电阻,CPEdl为恒相元件。
界面双电层电容Cdl和EIS 测得的缓蚀率IE分别根据式(7)和式(8)算得[3,21]:

表3 不同缓蚀剂浓度下的电化学阻抗谱参数Table 3 Parameters of the electrochemical impedance spectra at different corrosion inhibitor concentrations

图6 不同FFA 投加量下试样在1 mol/L HCl 中的Nyquist 谱和Bode 谱Fig. 6 Nyquist and Bode spectra of samples in 1 mol/L HCl solutions at different FFA dosages

图7 电化学阻抗谱模拟等效电路Fig. 7 Equivalent circuit for fitting the electrochemical impedance spectra
式中,Y0为CPE常数值,fmax为Nyquist 曲线上虚部最大值对应的频率,n为CPE 指数,和Rt分别为不含和含FFA 时试样的电荷转移电阻。
从中国知网的查询结果来看,至2016年6月,关于水利风景区旅游解说系统的文章只有1篇,即由戚均慧,钟林生,张生瑞,王英杰撰写的“水利风景区旅游解说系统的构建探讨——以甘肃冶力关国家水利风景区为例”。[7]该文章遵循注意特色、服务与教育并重、结合自然等原则,从游客,游客特征,水利风景区系统管理,解说方法等方面提出了水利风景区旅游解说系统构建路径和模式。
如图6a 所示,含和不含FFA 情况下的阻抗谱均为一个近半圆形容抗弧,外观没有发生变化,这说明HCl对碳钢试片的腐蚀机理并没有因为投加FFA 引起的腐蚀速率的降低而发生改变,也进一步证实20 碳钢电极表面的腐蚀过程主要受电荷转移控制[9]。
容抗弧直径越大,腐蚀速率越小,说明吸附在样品表面的FFA 形成了保护膜,抑制了腐蚀的发生。
从图6a 可以看出,当FFA 的投加量为5 g/L 时,容抗弧的直径最大,缓蚀率最大[3]。
从图6b 可以看出,随着FFA 的加入,阻抗增加,相位角也增加,FFA 投加量为5 g/L 时达到最大值。这表明该条件下样品表面吸附的FFA 分子最多,表面最均匀[19]。
这个结果也与失重实验的结果相一致,印证了实验结果的准确性。
表3 中,IE和η分别为室温下(298 K)通过EIS 测试和失重实验测得的缓蚀率,二者相差很小。
由表3可知,随着投加量的增加,Rt增加,说明腐蚀受到抑制;
FFA 投加量为5 g/L 时,IE达到最大值。
随着Rt的增加,Y0、Cdl降低,说明局部介电常数降低或双电层厚度增加,进一步证明缓蚀剂吸附在碳钢上,样品表面的水分子被替换,腐蚀反应程度降低[16]。
图8 为浸入不含有和含有5 g/L FFA 的1.0 mol/L HCl 中后试样表面接触角示意图。
表4 为浸入不含和含有5 g/L FFA 的1.0 mol/L HCl 中后试样表面接触角值。
由图8a 可知,在未添加FFA 的情况下,试片表面表现出亲水性。
这是试样在酸性介质中被腐蚀,导致表面粗糙度增加导致的。
在投加缓蚀剂的情况下,试样表面表现出疏水性。
接触角的显著增加表明,其表面形成了一层疏水膜,这可以归因于FFA 吸附的影响[20]。
由表4 可知,试样在含5 g/L FFA 的1 mol/L HCl 中腐蚀后,表面不同位置接触角的变化较小,说明形成的疏水膜较为均匀。

图8 浸入不含有和含有5 g/L FFA 的1 mol/L HCl 中后试样表面接触角示意图Fig. 8 Schematic diagram of contact angles measured on the coupon surfaces after submersion in 1 mol/L HCl without and with 5 g/L FFA corrosion inhibitor

表4 浸入不含和含有5 g/L FFA 的1 mol/L HCl 中后试样表面接触角值Table 4 Contact angle values measured on the sample surfaces after submersion in 1 mol/L HCl without and with 5 g/L FFA corrosion inhibitor
碳钢试片表面的SEM 形貌如图9 所示。
图9a 表明经过抛光的碳钢表面光滑平整,磨痕清晰。
在1 mol/L HCl 中腐蚀4 h 后(图9b),能够观察到碳钢表面被黑色不均匀的腐蚀产物(铁的氧化物或氢氧化物)膜覆盖[22],有蚀坑,腐蚀情况严重。
由图9c 可知,在含5 g/L FFA 的1 mol/L HCl 溶液中腐蚀4 h 后,碳钢表面趋于光滑平坦,没有明显的腐蚀现象,缓蚀剂均匀地分布在试样表面,甚至可以看到抛光打磨的痕迹。
因此,可以推断FFA 被吸附在碳钢表面形成了保护膜,覆盖了反应活性中心,有效地阻隔了盐酸与金属表面接触,从而抑制碳钢的腐蚀。
图9d 的FFA 投加量为10 g/L,由图9d 可知,碳钢表面未发生严重腐蚀,但成膜不均匀,在部分吸附膜的褶皱处存在蚀坑,这与2.2 节中的分析结果相一致,投加量过多时,分子之间的斥力增加,使得形成的吸附膜不均匀,未被保护的位置与腐蚀介质直接接触,因此,当投加量超过吸附平衡时的投加量时,缓蚀率呈现下降的趋势。

图9 碳钢试样表面SEM 形貌Fig. 9 SEM morphologies of carbon steel surfaces
图10 为20 钢表面的2D 和3D AFM 形貌。
由图10a 可知,未投加FFA 时,试片表面非常粗糙,表明试样腐蚀严重,计算得出的平均表面粗糙度为406 nm。而在存在FFA 的情况下,表面形态得到了显著的改善(图10b),平均粗糙度降低至51.9 nm,减少了87.2%,这进一步证实了FFA 对20 碳钢表面具有保护作用。

图10 浸入不含和含5 g/L FFA 的1 mol/L HCl 中后的碳钢表面的2D 和3D AFM 形貌Fig. 10 2D and 3D AFM morphologies of carbon steel surfaces after submersion in 1 mol/L without and with 5 g/L FFA inhibitor
(1)研发的环保缓蚀剂FFA 在温度为343 K、投加量为5 g/L 时,缓蚀率达到94.5%。
(2)吸附等温线的拟合结果表明吸附过程符合Langmuir 模型,吸附过程为吸热过程;
吸附机制为物理吸附和化学吸附共同作用。
(4)接触角测试结果表明,缓蚀剂在碳钢试片表面形成了均匀的疏水膜。
(5)SEM、AFM 测试进一步证实了缓蚀剂在盐酸环境中对20 碳钢表面具有优异的保护效果。
(6)FFA 拓宽了有机胺的应用范围,后续可深入探究其阻垢性能和机理,优化制备方案。
猜你喜欢试片碳钢缓蚀剂不同浓度的缓蚀剂对水轮机常用低合金钢的腐蚀防护研究大电机技术(2022年3期)2022-08-06一种基于多电极体系的新型顶部腐蚀监测传感器腐蚀与防护(2021年8期)2021-09-073种类型石油酸的腐蚀性以及相互影响石油学报(石油加工)(2021年3期)2021-05-14JRHS-2二氧化碳缓蚀剂的研究与应用云南化工(2020年11期)2021-01-14轴承钢GCr15SiMn试片与渗碳钢G20Cr2Ni4A试片接触疲劳寿命分析哈尔滨轴承(2020年1期)2020-11-03高钛普碳钢的生产实践山东冶金(2019年6期)2020-01-06油田埋地碳钢管道外腐蚀行为研究西南石油大学学报(自然科学版)(2018年4期)2018-08-02通过焊接与轧制制备的不锈钢/碳钢复合板的组织与性能焊接(2015年2期)2015-07-18碳钢在三种大气环境中的应力腐蚀装备环境工程(2015年4期)2015-02-28曼尼希碱型酸化缓蚀剂研究进展应用化工(2014年1期)2014-08-16扩展阅读文章
推荐阅读文章
老骥秘书网 https://www.round-online.com
Copyright © 2002-2018 . 老骥秘书网 版权所有